Los temas de Física y Fisicoquímica de la Secundaria en la Pcia de Buenos Aires, Argentina. Contenidos de la Dirección General de Escuelas
Física de 4to año
domingo, 19 de agosto de 2012
Los cambios físicos y químicos
Los cambios físicos y químicos
Reacciones químicas
Combustión: es una reacción química de oxidación, en la cual generalmente se desprende una gran cantidad de energía, en forma de calor y luz, manifestándose visualmente como fuego.
En toda combustión existe un elemento que arde (combustible) y otro que produce la combustión (comburente), generalmente oxígeno en forma de O2 gaseoso. Los explosivos tienen oxígeno ligado químicamente por lo que no necesitan el oxígeno del aire para realizar la combustión.
Los tipos más frecuentes de combustible son los materiales orgánicos que contienen carbono e hidrógeno. En una reacción completa todos los elementos tienen el mayor estado de oxidación. Los productos que se forman son el dióxido de carbono (CO2) y el agua, el dióxido de azufre (SO2) (si el combustible contiene azufre) y pueden aparecer óxidos de nitrógeno (NOx), dependiendo de la temperatura y la cantidad de oxígeno en la reacción.
En la combustión incompleta los productos que se queman pueden no reaccionar con el mayor estado de oxidación, debido a que el comburente y el combustible no están en la proporción adecuada, dando como resultado compuestos como el monóxido de carbono (CO). Además, pueden generarse cenizas.
El proceso de destruir materiales por combustión se conoce como incineración.
Para iniciar la combustión de cualquier combustible, es necesario alcanzar una temperatura mínima, llamada temperatura de ignición, que se define como, a la temperatura mínima necesaria para que los vapores generados por un combustible comiencen a arder o hervir depende de su temperatura y se parece a una sustancia pura, o combinada y eso lo convierte en un cambio químico – físico, se mide en °C.
La temperatura de inflamación, en °C y a 1 atm es aquella temperatura a la que un combustible emite gases inflamables suficientes para alcanzar en su atmósfera el límite inferior de inflamabilidad, a partir del cual, con una fuente de calor externa puede producirse una combustión no auto mantenida. a la que, una vez encendidos los vapores del combustible, éstos continúan por si mismos el proceso de combustión.
Biomasa es el término utilizado para describir la materia orgánica no fosilizada en un proceso biológico espontaneo o provocado, utilizado como fuente de energía aunque puede tener uso industriales.
—La biomasa contiene carbono, nitrógeno, oxigeno e hidrogeno como cada ser vivo, y por lo tanto presentara el potencial para la combustión. Esta combustión entonces ofrecerá la energía en forma de calor y electricidad.
La energía generada a partir de la biomasa es una de las formas más prometedoras de reducir, en cantidades importantes, el dióxido de Carbono, proveniente de la combustión del carbón y el gas natural.
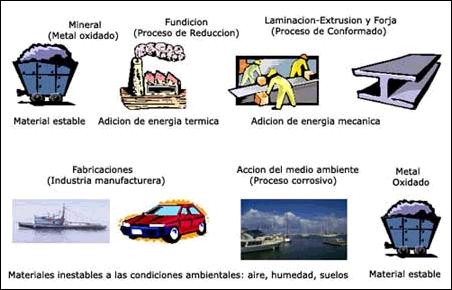
Corrosión: es una reacción química (oxido reducción) en la que intervienen 3 factores: la pieza manufacturada, el ambiente y el agua, o por medio de una reacción electroquímica.
Los factores más conocidos son las alteraciones químicas de los metales a causa del aire, como la herrumbre del hierro y el acero (es una aleación de hierro con una cantidad de carbono variable) o la formación de pátina verde en el cobre y sus aleaciones; de cobre y estaño (bronce) y de cobre y zinc (latón).
Sin embargo, la corrosión es un fenómeno mucho más amplio que afecta a todos los materiales (metales, cerámicas, polímeros, etc.) y todos los ambientes (medios acuosos, atmósfera, alta temperatura, etc.).
Es un problema industrial importante, pues puede causar accidentes (ruptura de una pieza) y, además, representa un costo importante, ya que se calcula que cada pocos segundos se disuelven 5 toneladas de acero en el mundo.
La reacción de síntesis o reacción de combinación es aquella en que dos elementos o compuestos reaccionan para generar un solo producto.
Algunas reacciones de síntesis se dan al combinar un óxido básico con agua, para formar un hidróxido, o al combinar el óxido de un no metal con agua para producir un oxido ácido.
La descomposición química es un proceso que experimentan algunos compuestos químicos en el que, de modo espontáneo o provocado por algún agente externo, a partir de una sustancia compuesta se originan dos o más sustancias de estructura química más simple. Es el proceso opuesto a la síntesis química.
La descomposición química es, con frecuencia, una reacción química no deseada, pues la estabilidad de un compuesto es siempre limitada cuando se le expone a condiciones ambientales extremas como el calor, la electricidad, las radiaciones, la humedad o ciertos compuestos químicos (ácidos, oxidantes, etc). Los casos más frecuentes de descomposición son la descomposición térmica y la electrólisis. La descomposición química total de un compuesto origina los elementos que lo constituyen.
Ecuaciones químicas
Una reacción ácido-base es una reacción química que ocurre entre un ácido que es cualquier compuesto químico que, cuando se disuelve en agua, produce una solución con cationes y una base que es cualquier sustancia que en disolución acuosa aporta iones OH− al medio.
La lluvia ácida se forma cuando la humedad en el aire se combina con los óxidos de nitrógeno y el dióxido de azufre emitidos por fábricas, centrales eléctricas y vehículos que queman carbón o productos derivados del petróleo. En interacción con el vapor de agua, estos gases forman ácido sulfúrico y ácidos nítricos, finalmente, estas sustancias químicas caen a la tierra acompañando a las precipitaciones.
Los contaminantes atmosféricos primarios que dan origen a la lluvia ácida pueden recorrer grandes distancias, siendo trasladados por los vientos cientos o miles de kilómetros antes de precipitar en forma de rocío, lluvia, llovizna, granizo, nieve, niebla o neblina. Cuando la precipitación se produce, puede provocar importantes deterioros en el ambiente.
La lluvia normalmente presenta un pH de aproximadamente 5.65 (ligeramente ácido), debido a la presencia del CO2 atmosférico, que forma ácido carbónico, H2CO3. Se considera lluvia ácida si presenta un pH de menos de 5 y puede alcanzar el pH del vinagre (pH 3). Estos valores de pH se alcanzan por la presencia de ácidos como el ácido sulfúrico, H2SO4, y el ácido nítrico, HNO3. Estos ácidos se forman a partir del dióxido de azufre, SO2, y el monóxido de nitrógeno que se convierten en ácidos.
Un precipitado es el sólido que se produce en una disolución por efecto de difusión o de una reacción química o bioquímica. A este proceso se le llama reacciones de precipitación. Dicha reacción puede ocurrir cuando una sustancia insoluble se forma en la disolución debido a una reacción química o a que la disolución ha sido sobresaturada por algún compuesto, esto es, que no acepta más soluto y que al no poder ser disuelto, dicho soluto forma el precipitado.
En la mayoría de los casos, el precipitado (el sólido formado) cae al fondo de la disolución, aunque esto depende de la densidad del precipitado: si el precipitado es más denso que el resto de la disolución, cae. Si es menos denso, flota, y si tiene una densidad similar, se queda en suspensión.
El efecto de la precipitación es muy útil en muchas aplicaciones, tanto industriales como científicas, en las que una reacción química produce sólidos que después puedan ser recogidos por diversos métodos, como la filtración, la decantación o por un proceso de centrifugado.
Reacciones de Óxido-reducción o REDOX: Se denomina reacción de reducción-oxidación, de óxido-reducción o, simplemente, reacción REDOX, a toda reacción química en la que uno o más pares de electrones se transfieren entre los reactivos, provocando un cambio en sus estados de oxidación.
Para que exista una reacción de reducción-oxidación, en el sistema debe haber un elemento que ceda electrones, y otro que los acepte:
El agente reductor es aquel elemento químico que suministra electrones de su estructura química al medio, aumentando su estado de oxidación, es decir, siendo oxidado.
El agente oxidante es el elemento químico que tiende a captar esos electrones, quedando con un estado de oxidación inferior al que tenía, es decir, siendo reducido.
Cuando un elemento químico reductor cede electrones al medio, se convierte en un elemento oxidado, y la relación que guarda con su precursor queda establecida mediante lo que se llama un «par redox». Análogamente, se dice que, cuando un elemento químico capta electrones del medio, este se convierte en un elemento reducido, e igualmente forma un par redox con su precursor oxidado.
Se llama energía de una reacción química a la energía absorbida o desprendida en la misma por el sistema reactivo.
El valor de la energía de reacción depende de las condiciones de presión y temperatura y de la cantidad de sustancia que se transforma. Los valores de la energía de reacción se expresan por mol de producto formado o reactivo gastado y, generalmente, en condiciones normales: 1 atm y 298 K (25 °C). Se conoce como calor de reacción, ya que se manifiesta de esta forma.
En las reacciones endotérmicas, los productos tienen mayor energía que los reactivos; por ello, debemos comunicar energía a la reacción. La reacción solo tendrá lugar mientras se le suministre dicha cantidad de energía; en el momento en el que no absorba tal cantidad de energía, la reacción se detendrá.
En las reacciones exotérmicas, los productos tienen menos energía que los reactivos, por lo que se desprende energía.
Suscribirse a:
Entradas (Atom)